mdd法规(mdd法规的全称)
阿拉伯安全性及有效性提供一整套全国性的方案2002年澳大利亚颁布mdd法规了医疗器械法规2002mdd法规,这是一部医疗器械管理方面的专门法规TGA执行治疗用品法案医疗器械法规2002所赋予的产品市场准入和市场监管的职责,并保证在澳大利亚上市的医疗器械符合标准,并保证进一步地发展澳大利亚的治疗水平以及医疗器械。
1需向制造商确认其符合性声明和技术文件已经拟定,且在适当时核实其已实施适当的符合性评估流程2需保留一份可用的技术文件欧盟符合性声明副本如适用,需保留一份关于产品的相关证书副本3欧盟授权代表自身应遵守IVDR法规中的注册义务,同时应确认制造商已遵守法规中所规定的的注册义务4。
1996版标准YYT0287 和YYT0288,对医疗器械生产企业的质量管理体系提出了专用要求,为医疗器械的质量达到安全有效起到了很好的促进作用。
从性质上而言,物权不能适用诉讼时效的规定物权请求权是以物权为基础而产生的权利其产生根据在于物权是对客体进行支配并排斥他人干涉的权利,当物权人的支配权受到他人侵害时,为恢复权利人对客体的圆满支配状态,物权人才应行使此项请求权物被他人以占有以外的其它非法方式妨害的,物权人可以行使物权。
hbjmddcl 采纳率54% 擅长 烦恼 生活 文化艺术 其他回答 少先队员应该怎么做mdd法规我想,作为一个少先队员,首先要做到对老师的尊重,对同学的礼貌讲信用文明做事,积极向上,热爱祖国,不破坏公物,这些都是少先队员最起码的修养其次,少先队员要做同学们的好榜样,多提醒别人要文明礼貌,不打闹随意骂人牢记“八荣。
医疗器械在国际上不仅只是一般的上市商品在商业环境中运行,它还要受到国家和地区法律法规的监督管理,如美国的FDA欧盟的MDD欧盟医疗器械指令中国的医疗器械监管条例因此,该标准必须受法律约束,在法规环境下运行,同时必须充分考虑医疗器械产品的风险,要求在医疗器械产品实现全过程中进行风险。
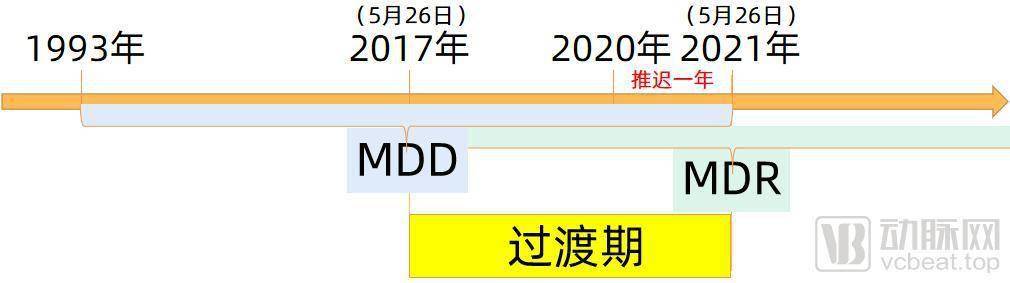
MDR医疗器械监管的新挑战 自2017年欧洲医疗器械法规MDR取代MDD和AIMD指令以来,全球医疗行业面临着一场深刻的转型MDR的实施不仅强化了医疗器械制造商的责任,还对医疗器械的分类监管标准和临床评估带来了显著的变化MDR将医疗器械划分为MDIIII类和IVDAD类,每个类别都要求更高的透明度。
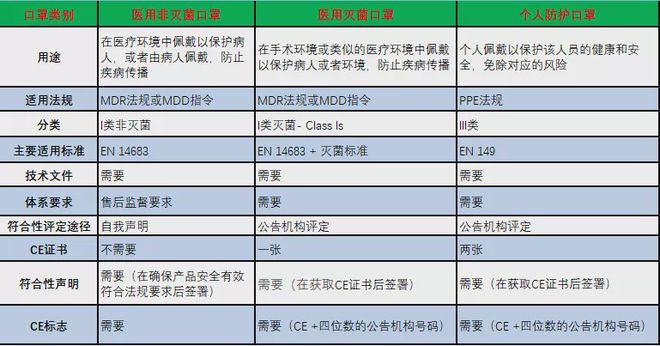
3欧盟MDD认证MDD是欧盟医疗器械9342EEC指令的简称,适用于在欧盟国家销售的医疗器械进行认证,是强制认证,需要由获得授权的公告机构进行认证,例如TUV瑞士SGS等MDD是英文缩写了,M医疗D器械D指令欧盟CE认证下面的一个指令,针对医疗器械的MDD指令的产品分3个等级一类,二类,三类,危险。
对于医疗器械,现行有三个指令1医疗器械指令MDD 9342EEC2体外诊断医疗器械指令IVDD 9879EC 3有源植入医疗器械指令AIMD 90385EEC自2020526, 上述MDD和AIMD指令失效, 开始强制执行以下法规MDR 法规 2017745自2022526,上述IVDD指令失效, 开始强制执行以下法规IVDR 法规。